Notizen aus dem Labor: T-Zell-Engager, die nächste Stufe der Krebsimmuntherapie?

Von Paul Bunk, Doktorand, Cold Springs Harbor Laboratory
Im Januar 2022 wurde Tebentafusp-tebn, auch bekannt unter dem leichter auszusprechenden Markennamen Kimmtrakwurde für die Behandlung von nicht resektablen oder metastasierten Uvea- Melanom. Diese Behandlung ist die erste und bislang einzige von der FDA zugelassene Therapie für diese seltene Art von Krebs. Tebentafusp-tebn („tebe“) ist auch ein Beispiel für eine wachsende neue Klasse von Immuntherapien, genannt bispezifische T-Zell-Engager, zu denen auch das Leukämiemedikament Blinatumomab (Blincyto) gehört. Aber was sind T-Zell-Engager, wie wirken sie und warum haben sie sich jetzt bei metastasiertem Aderhautmelanom als wirksam erwiesen, einem Krebs, der gegen andere derzeit verfügbare Immuntherapien resistent zu sein scheint?
Wie T-Zellen Krebs erkennen
Um die T-Zell-Aktivatoren zu verstehen, müssen wir zunächst die adaptiven ImmunsystemsDie Aufgabe des adaptiven Immunsystems besteht darin, alles zu erkennen und zu beseitigen, was dem Körper schaden kann, darunter Krankheitserreger wie Bakterien und Viren, aber auch Tumore. T-Zellen sind Teil des adaptiven Immunsystems und haben die Aufgabe, Krebszellen oder infizierte Zellen direkt abzutöten.
Das adaptive Immunsystem unterscheidet im Allgemeinen zwischen Eigenem und Fremdem – mit anderen Worten, es unterscheidet zwischen gesunden Zellen des Individuums und Krebszellen oder infizierten Zellen, die eine Bedrohung darstellen. T-Zellen unterscheiden Eigenes und Fremdes, indem sie Proteinfragmente erkennen – wir nennen diese Peptide –, die den T-Zellen von MHC-Molekülen (Haupthistokompatibilitätskomplex) auf der Oberfläche von Zellen präsentiert werden. Diese MHC-Moleküle kontrollieren streng die Erkennung beschädigter oder mutierter Peptiden von infizierten oder maligne Zellen durch T-Zellen. Bei Infektionen führt die Identifizierung und Zerstörung infizierter Zellen durch T-Zellen zu einer schnellen und starken Immunantwort, da in Viren Peptide vorhanden sind, die sich stark von denen gesunder menschlicher Zellen unterscheiden.
Bei Krebs ist die Identifizierung und Zerstörung der bösartigen Zellen weniger effizient, da menschliche Krebszellen nur eine begrenzte Anzahl von Peptiden besitzen, die T-Zellen als fremd erkennen können. Zudem fehlen ihnen oft die MHC-Moleküle, die erforderlich sind, um diese Peptide den T-Zellen zu präsentieren. Einige Tumoren weisen eine große Anzahl von Mutationen auf, oft aufgrund hoher Konzentrationen von DNA Schäden oder Mangel an Enzymen, die DNA reparieren. Dies führt dazu, dass viele krebsreaktive T-Zellen in die Tumor und töten die Tumorzellen, indem sie ihre mutierten Peptide erkennen. Diese Art von Krebs nennen wir immunologisch „heiß“. Andere Tumoren haben nur eine geringe Anzahl von Mutationen – was wir als geringe Mutationslast bezeichnen – und werden aufgrund der geringen Anzahl von T-Zellen im Tumor immunologisch „kalt“ genannt. Dieses Fehlen von T-Zellen ist auf die geringe Mutationslast zurückzuführen, die dazu führt, dass nur wenige mutierte Peptide von T-Zellen erkannt werden können.
Neben dem Mangel an immunogenen Peptiden in vielen Tumoren haben T-Zellen oft mit anderen Hürden zu kämpfen, die ihre Fähigkeit einschränken, in den Tumor einzudringen und Krebszellen zu töten. Selbst wenn ein Krebs beispielsweise eine hohe Mutationslast und viele krebsreaktive T-Zellen aufweist, verlieren diese T-Zellen oft ihre Fähigkeit, Krebszellen im Tumor richtig anzugreifen. Diese Immun-„Dysfunktion“ wird durch eine Reihe von Mechanismen verursacht, darunter Tumore, die das Immunsystem dazu veranlassen, T-Zellen zu „bremsen“ (oft als „Checkpoints“ bezeichnet). Diese „Immun-Checkpoints“ sind wichtig, um gesundes, normales Gewebe vor immunvermittelten Schäden zu schützen (die bei Autoimmunerkrankungen auftreten, darunter Krankheiten wie Lupus, rheumatoide Arthritis und Multiple Sklerose). Im Zusammenhang mit Krebs werden Immun-Checkpoints jedoch von Krebszellen ausgenutzt, um sich vor der Zerstörung durch das Immunsystem zu schützen. Das Wissen, dass Tumore diese „Bremsen“ nutzen und wie sie innerhalb der T-Zelle und in Tumoren funktionieren, führte zu nobelpreisgekrönter Forschung und der Entwicklung einer Art von Immuntherapie Immun-Checkpoint-Blockade genannt. Sie kennen vielleicht einige der häufig verwendeten Medikamente zur Immun-Checkpoint-Blockade, darunter Ipilimumab (Yervoy), Nivolumab (Opdivo), Pembrolizumab (Keytruda), Cemiplimab (Libtayo), Atezolizumab (Tecentriq), Avelumab (Bavencio) und Durvalumab (Imfinzi). Diese Medikamente blockieren die Immuncheckpoints und lösen die „Bremsen“ des Immunsystems, wodurch die T-Zellen wiederbelebt werden, sodass sie mutierte Peptide im Tumor erkennen, den anderen unterdrückenden Faktoren im Tumor widerstehen und die Krebszellen abtöten können.
Kommen wir nun auf unsere beiden Krebsarten zurück – immunologisch „heiße“ Tumoren mit einer hohen Mutationszahl und immunologisch „kalte“ Tumoren mit einer geringen Mutationszahl: Bei immunologisch „heißen“ Tumoren besteht eine bestehende T-Zell-Reaktion gegen die Krebszellen, die durch eine Immun-Checkpoint-Blockade ausgelöst werden kann. Kutanes Melanomweist beispielsweise eine hohe Anzahl von Mutationen auf; dieser immunologisch „heiße“ Status erklärt, warum die Blockade von Immuncheckpoints bei vielen Patienten mit Haut- Melanom.
Das Aderhautmelanom hingegen weist eine geringe Mutationslast auf, was bedeutet, dass es nicht viele mutierte Peptide gibt, die die T-Zellen erkennen und gegen die sie reagieren könnten. Infolgedessen sind im Tumor nicht viele T-Zellen vorhanden. Das Aderhautmelanom wird daher als immunologisch „kalt“ bezeichnet und reagiert nicht gut auf eine Immun-Checkpoint-Blockade, da nicht genügend bereits vorhandene T-Zellen vorhanden sind, um den Krebs anzugreifen, selbst wenn die „Bremsen“ gelöst wurden. Darüber hinaus befinden sich auf den Krebszellen nicht genügend mutierte Peptide, damit die wenigen vorhandenen T-Zellen den Krebs erkennen und seine Zerstörung einleiten können.
Die Prognose für Patienten mit Aderhautmelanom hat sich seit Jahrzehnten nicht verbessert. Mit der Zulassung von Tebe, einem neuen Typ eines bispezifischen T-Zell-Aktivators, durch die FDA könnte sich das Blatt jedoch wenden.
T-Zell-Aktivatoren bringen T-Zellen dazu, Krebszellen zu töten, indem sie sie einander näher bringen
Wie also bewirken T-Zell-Aktivatoren das Absterben von Krebszellen? Wie oben beschrieben, sind T-Zellen Teil unseres adaptiven Immunsystems und können Krebszellen direkt abtöten, wenn sie diese Zellen anhand ihrer mutierten Peptide erkennen, die vom MHC-Molekül auf den bösartigen Zellen präsentiert werden. Dieser Prozess ist wirksam, wenn die Mutationslast hoch ist und viele mutierte Peptide erkannt werden müssen, wie bei kutanem Melanom. In Tumoren mit geringer Mutationslast erkennen T-Zellen Krebszellen jedoch einfach nicht als Bedrohung, da sie aufgrund ihres Mangels an mutierten Peptiden wie gesunde Zellen erscheinen.
Hier kommen bispezifische T-Zell-Engager ins Spiel. T-Zell-Engager sind große Moleküle mit zwei Teilen, von denen einer spezifisch an Krebszellen bindet, während der andere spezifisch an T-Zellen bindet und diese stimuliert. T-Zell-Engager werden intravenös verabreicht und zirkulieren dann im Blutkreislauf, bis sie auf einen Tumor treffen. Zelle die anzeigen Antigen vom T-Zell-Engager erkannt. Sobald der T-Zell-Bindungsteil des Engagers mit der Tumorzelle verbunden ist, kann er sich an jede T-Zelle in der Nähe binden. Durch dieses Bindungsereignis bleibt die T-Zelle in unmittelbarer Nähe der Krebszelle und aktiviert ihre biochemische Maschinerie, um die erforderlichen Schritte zum Abtöten der bösartigen Zellen durchzuführen.
Auf molekularer Ebene ist dies alles möglich, weil die beiden „bindenden“ Teile des T-Zell-Engagers jeweils nur an eine bestimmte Art von Protein. Der „krebsspezifische“ Teil des T-Zell-Engagers bindet an Proteine, die nur auf Tumorzellen vorhanden sind. Wir nennen diese krebsspezifischen Proteine Tumorassoziierte Antigene (TAAs). Der „T-Zell-spezifische“ Teil des T-Zell-Aktivators bindet an ein Protein namens CD3, das auf allen T-Zellen exprimiert wird (siehe Abb. 1).
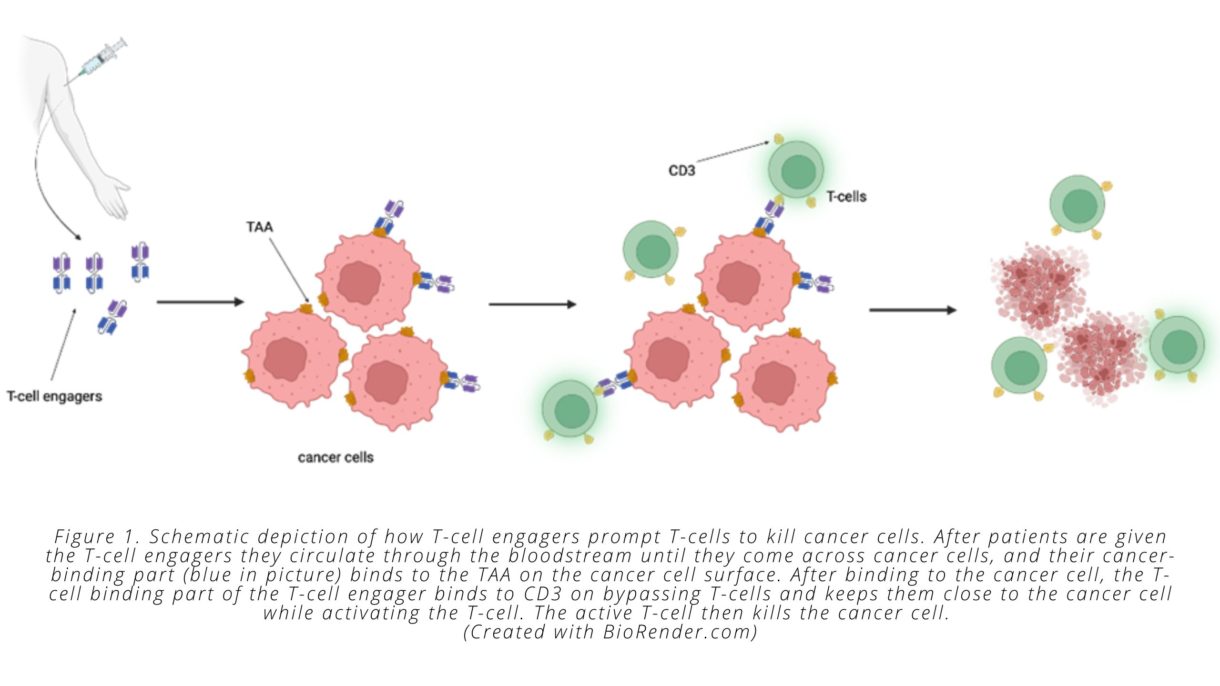
Wichtig ist, dass T-Zell-Engager eine der Herausforderungen überwinden können, die mit immunologisch „kalten“ Tumoren verbunden sind. Wie oben erwähnt, enthalten diese Tumorarten keine vorbestehende krebsspezifische Immunreaktion – das heißt, sie haben keine Masse dysfunktionaler krebsspezifischer T-Zellen – die durch Immun-Checkpoint-Inhibitoren wiederbelebt werden können. T-Zell-Engager umgehen dieses Problem, indem sie nicht-tumorspezifische T-Zellen dazu veranlassen, die Krebszellen anzugreifen. Dieser Prozess bedeutet, dass T-Zellen durch den bispezifischen Engager gegen Krebszellen umgeleitet werden können, unabhängig davon, ob die T-Zelle andernfalls ein mutiertes Krebszellpeptid erkannt hätte, da der T-Zell-Engager das von der Krebszelle präsentierte TAA erkennt und die T-Zelle durch Bindung an CD3 aktiviert. Sobald T-Zellen aktiviert und dazu gebracht wurden, Krebszellen abzutöten, sondern sie Moleküle ab, die andere T-Zellen rekrutieren, was wiederum dazu führt, dass mehr und mehr Immunzellen in den Tumor eindringen – ein weiterer Weg, mit dem T-Zell-Aktivatoren die Probleme lösen, die mit „kalten“ Tumoren verbunden sind.
Um es noch einmal zusammenzufassen: T-Zellen sind Immunzellen, die Krebszellen töten können, wenn sie mutierte Peptide auf der Oberfläche der Krebszellen erkennen, die die Krebszelle von einer gesunden Zelle unterscheiden. Aber immunologisch „kalte“ Krebsarten haben nur wenige Mutationen und daher eine geringe Anzahl mutierter Peptide, die von den T-Zellen erkannt werden können. Außerdem sind bei diesen Krebsarten oft nur wenige T-Zellen im Tumor vorhanden, was zu einem niedrigen Verhältnis von T-Zellen zu Tumorzellen und einer schlechten T-Zell-Tötung des Tumors führt. Bispezifische T-Zell-Engager sind Medikamente, die diese Probleme lösen sollen, indem sie T-Zellen auf Tumorantigene umlenken und T-Zellen stimulieren, Tumorzellen zu töten. Der Engagierer bringt diese beiden Zellen nah zusammen und aktiviert die T-Zellen, sodass die T-Zellen die Krebszellen töten können. Sie können sehen, wie der Name bispezifischer T-Zell-Angreifer ist eine treffende Beschreibung des Medikaments, da es sich „spezifisch“ an zwei („bi“) Zelltypen bindet und T-Zellen „aktiviert“, um Krebszellen abzutöten.
Ein neuer Typ von T-Zell-Aktivator kommt in die Klinik
Die oben beschriebenen bispezifischen T-Zell-Engager – darunter Blinatumomab, ein Engager, der T-Zellen zum CD19-Protein auf B-Zell-Leukämiezellen lenkt – sind so konstruiert, dass sie die bösartigen Zellen durch eine antikörperbasierte Struktur erkennen. Sie funktionieren, weil Antikörper kann Proteine (die TAAs) spezifisch erkennen und daran binden an der Oberfläche von Krebszellen.
Leider sind bei der Krebsimmuntherapie nur 10 % aller Proteine auf der Oberfläche einer Zelle vorhanden und stehen für antikörperbasierte T-Zell-Aktivatoren zur Erkennung und Bindung zur Verfügung. Das bedeutet, dass 90 % der Proteine – und damit 90 % der Marker, die zwischen Krebszellen und gesunden Zellen unterscheiden – nur auf der Oberfläche vorhanden sind. innerhalb einer Krebszelle. Viele Krebsarten würden also nicht auf einen bispezifischen T-Zell-Engager reagieren, da dieser nicht in der Lage wäre, eine TAA zu identifizieren. an der Oberfläche der Krebszelle, um sie von gesunden Zellen zu unterscheiden. Aber was wäre, wenn wir die 90% der Proteine gezielt anvisieren könnten, innerhalb der Zelle als mögliche TAAs, sodass T-Zell-Aktivatoren die Krebszelle identifizieren und sich an sie binden können?
Hier kommt die Innovation rund um tebe ins Spiel. Anders als die ersten T-Zell-Engager, die zwei Antikörper verwenden, nutzen tebe und andere T-Zell-Engager, die sich derzeit in der Entwicklung befinden, einen T-Zell- Rezeptor Struktur anstelle eines Antikörpers, um ein Peptid zu erkennen, das vom MHC auf der Oberfläche von Tumorzellen angezeigt wird. Die andere Seite, der Teil des T-Zell-Engagers, der an CD3 auf T-Zellen bindet, ist ein Antikörper, der CD3 stimuliert, was für die Aktivierung der T-Zellen wichtig ist. Die Verwendung von T-Zell-Rezeptoren als Teil eines T-Zell-Engagers ermöglicht es dem Engager daher, an TAAs zu binden, die für antikörperbasierte T-Zell-Engager wie Blinatumomab nicht zugänglich wären. Dieser Unterschied ist entscheidend für die Behandlung von Krebsarten, bei denen sich keine oder nur wenige TAAs auf der Zelloberfläche befinden – wie etwa beim Aderhautmelanom. Sobald T-Zellen durch einen T-Zell-Engager aktiviert werden und beginnen, Krebszellen zu zerstören, werden Signale freigesetzt, die nahegelegene T-Zellen warnen, dass Krebszellen vorhanden sind, was zu einer Kaskade von T-Zell-vermittelter Krebszellzerstörung führt.
Der krebsbindende Teil von Tebe zielt auf ein von TAA abgeleitetes Peptid namens gp100, ein Protein, das nur auf der Innenseite von Melanozyten und Melanomzellen. Ein Vorbehalt bei der Verwendung von T-Zell-Rezeptor-basierte bispezifische T-Zell-Aktivatoren ist, dass das MHC-Molekül (das zur Erkennung von Peptiden auf der Oberfläche von Krebszellen erforderlich ist) in vielen verschiedenen Formen vorkommt, die wir von unseren Eltern erben. Ein spezifischer T-Zell-Rezeptor kann nur Peptide erkennen, die auf ausgewählten MHC-Proteinen angezeigt werden. Tebe richtet sich gegen gp100, das von HLA-A*02:01 präsentiert wird, der häufigsten MHC-Variante, die jedoch nur bei etwa der Hälfte aller Menschen vorhanden ist. Um Tebe gegen fortgeschrittenes Aderhautmelanom zu erhalten, müssen Patienten auf das Vorhandensein von HLA-A*02:01 getestet werden, was für die Wirksamkeit des Medikaments erforderlich ist. Laufende Forschung wird wahrscheinlich andere Formen bispezifischer Engagierer entwickeln, die von verschiedenen MHC-Typen abhängen.
Ein erster Erfolg beim Aderhautmelanom
Die FDA-Zulassung von tebe basierte auf den Ergebnissen einer Phase 3 klinischen Studie in der das Medikament einen statistisch und klinisch bedeutsamen Vorteil beim Gesamtüberleben bei Patienten mit nicht resektablem oder metastasiertem Aderhautmelanom zeigte (Lesen Sie hier den veröffentlichten Artikel). Das Aderhautmelanom ist eine aggressive Form des Melanoms, die das Auge befällt und sich bei etwa der Hälfte der Patienten schließlich auf andere Körperteile ausbreitet, fast immer auf die Leber. Dieser Tumor ist sehr aggressiv und hat nur selten auf eine andere Form der Therapie reagiert, was ihn zu einem ungedeckten klinischen Bedarf macht, da Patienten derzeit im Durchschnitt nur ein Jahr nach der Behandlung überleben. Metastasierung diagnostiziert wird. Obwohl dieses Medikament das erste war, das für Aderhautmelanom zugelassen wurde, gibt es mehrere andere Behandlungen für Aderhautmelanom, die sich noch in klinischen Studien befinden. Diese Behandlungen umfassen Antikörper-Wirkstoff-Konjugate, Kombinationstherapien, Krebsimpfstoffeund adoptive T-Zelltherapien. Es bleibt abzuwarten, wie gut sich diese Ansätze in Studien bewähren.
Es gibt auch eine Reihe anderer T-Zell-Rezeptor-basierte bispezifische T-Zell-Aktivatoren derzeit in der Entwicklung, da auch andere Unternehmen an das Potenzial glauben, tumorspezifische Peptide anzugreifen, die aus Proteinen in Krebszellen gewonnen werden. Dazu gehören Immatics‘ IMA401 und IMA402, die bei einer Reihe solider Tumore wie nicht-kleinzelligem Lungenkrebs und Melanom getestet werden, sowie AbbVies ABBV-189, das ebenfalls bei verschiedenen Krebsarten getestet wird. Trotz dieser vielversprechenden ersten Zulassung eines Bispezifischer T-Zell-Aktivator auf Basis des T-Zell-Rezeptors, es bleiben jedoch Hindernisse bestehen. Wie bei anderen Immuntherapien entwickeln Tumore manchmal alternative Mechanismen, um der Immunreaktion zu widerstehen oder ihr zu entgehen und wachsen sogar nach anfänglicher Regression wieder nach. Derzeit laufen Forschungen, um bessere T-Zell-Aktivatoren und Kombinationen mit anderen Therapien zu entwickeln, um den Nutzen dieser neuartigen Immuntherapie zu erhöhen und Resistenzen und Entgehen gegenüber wirksamen Immuntherapien zu überwinden.

Paul Bunk ist Doktorand am Cold Spring Harbor Laboratory, einem in New York ansässigen Forschungsinstitut, das in den Bereichen Krebsbiologie, Neurowissenschaften und Pflanzenbiologie weltweit anerkannt ist. Paul arbeitet in der Gruppe von Semir Beyaz und konzentriert seine Forschung auf die Auswirkungen des Stoffwechsels auf Immunzellen und ihre Fähigkeit, Krebs zu bekämpfen. Mit dieser Forschung ist das Beyaz Lab führend in der Krebsforschung. Immunologie und hofft, dazu beizutragen, dass in Zukunft bessere Immuntherapien entwickelt werden.
Neueste Beiträge

Webinar zum Uveamelanom: Teil II – Therapiewege bei metastasiertem Melanom

Wade Watson, Überlebender eines Melanoms im Stadium III

Krebs ist mehr als eine Diagnose: Geist, Sinn und Heilung

Merlin CP-GEP ist der erste und einzige Genexpressionsprofiltest, der von NCCN® empfohlen wird.


